Pi retrodonacija
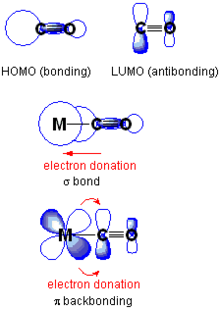
π retrodonacija je hemijski koncept koji označava pojavu da elektroni prelaze iz atomske orbitale jednog atoma u π* antivezujuću orbitalu drugog atoma ili liganda.[1][2] Ona je posebno zastupljena u organometalnoj hemiji prelaznih metala sa multiatomskim ligandima poput ugljen-monoksida, etilena ili nitrozonijum katjona. Elektroni metala se se koriste za vezivanje liganda, u procesu kojim se umanjuje metalni višak negativnog naelektrisanja. Jedinjenja u kojima se javlja π retrodonacija su između ostalog Ni(CO)4 i Zeisova so.
IUPAC opisuje retrodonaciju kao vezivanje π-konjugovanih liganda za prelazni metal pri čemu dolazi do sinergističkog procesa donacije elektrona sa popunjenih π-orbitala ili orbitala sa slobodnim elektronskim parom liganda u praznu orbitalu metala (donor–akceptor veza), zajedno sa oslobađanjem elektrona iz nd orbitale metala (koji ima π-simetriju u odnosu na metal–ligand osu) u prazne π*-antivezujuće orbitale liganda.[3]
Vidi još
- Teorija ligandnog polja
- Pravilo 18-elektrona
- Metalni karbonil
Reference
- ^ Miessler, Gary L.; Donald Arthur Tarr (1999). Inorganic Chemistry. ISBN 978-0-13-841891-5.
- ^ Cotton, Frank Albert; Wilkinson, Geoffrey; Carlos A. Murillo (1999). Advanced Inorganic Chemistry. ISBN 978-0-471-19957-1.
- ^ McNaught, A.; Wilkinson (2006). IUPAC. Compendium of Chemical Terminology, 2nd ed. (the "Gold Book"). Oxford: Blackwell Scientific Publications. ISBN 978-0-9678550-9-7. doi:10.1351/goldbook.
Literatura
- McNaught, A.; Wilkinson (2006). IUPAC. Compendium of Chemical Terminology, 2nd ed. (the "Gold Book"). Oxford: Blackwell Scientific Publications. ISBN 978-0-9678550-9-7. doi:10.1351/goldbook.
- п
- р
- у
- Brojanje elektrona
- pravilo 18-elektrona
- teorija poliedralnog skeletalnog elektronkog para
- izolobalni princip
- π retrodonacija
- haptičnost
- broj d electrona
- Spinska stanja
- Oksidativna adicija / reduktivna eliminacija
- migratorno umetanje
- β-hidridna eliminacija
- transmetalacija
- ugljenometalacija
- Gilmanovi reagensi
- Grinjarovi reagensi
- ciklopentadienilni kompleksi
- metaloceni
- sendvična jedinjenja
- kompleksi tranzicionih metalnih karbena
- kompleksi tranzicionih metalnih karbina
- Monsantov proces
- Zigler–Nata proces
- Shelov proces viših olefina
- olefinska metateza








